概要
核磁気共鳴(Nuclear Magnetic Resonance:NMR)法は、分子構造や様々な分子間相互作用、分子の運動状態などを調べる手法です。本講座では、分子運動性の評価や、定量測定での条件設定に必要な緩和時間について、その測定手法を含めて紹介します。
1.T1緩和時間とT2緩和時間
「NMR入門講座 ②溶液NMR測定法」で紹介しましたように、試料全体にラジオ波を照射すると、z軸上の巨視的磁化がxy平面へ倒れていきます(図1-(ⅱ))。巨視的磁化が倒れている途中でラジオ波の照射を止めると、傾いた巨視的磁化はz軸上の熱平衡状態に戻っていき(図1-(ⅲ))、これを緩和過程と呼びます【図1】。
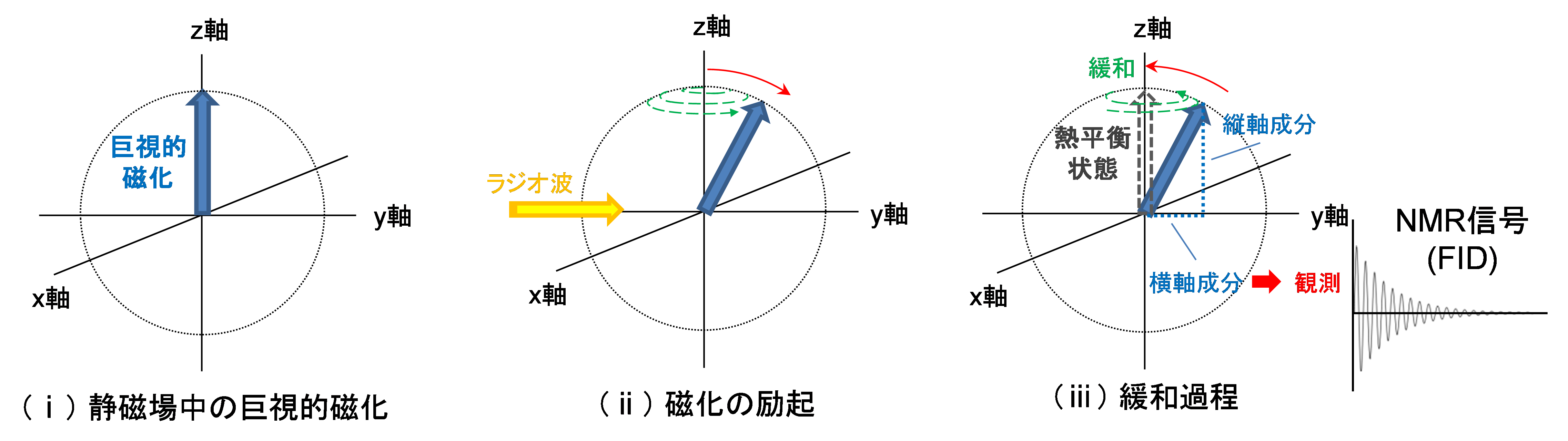
【図1】NMR測定での巨視的磁化の挙動
この緩和過程は2種類に分けられ、巨視的磁化の縦軸(z軸)方向成分が熱平衡状態に戻るまでの時間をT1緩和時間(スピン-格子緩和、縦緩和時間とも呼ばれる)、巨視的磁化のxy平面の横軸成分が0になるまでの時間の長さをT2緩和時間(スピン-スピン緩和、横緩和時間とも呼ばれる)と表現します。
T1緩和時間は巨視的磁化が熱平衡状態に戻るまでの時間を表し、定量測定に必要な待ち時間を決める目安となります。一般的に、90°パルスを完全に緩和させるには少なくとも5×T1秒待つ必要があると言われています。1)
一方、T2緩和時間はNMR信号(FID)の長さに影響し、T2緩和時間が長いほど、スペクトルの線幅は小さくなります。
また、緩和時間は回転相関時間τ cと【図2】の関係にあります。τ cは揺らいでいる分子が一つの状態に留まる平均時間を表し、値が大きいほど分子運動性は小さくなります。
溶液NMRでは分子運動性が高いため図の左側の運動領域となり、T1≒T2の関係になります。一方、固体NMRでは分子運動性が小さいため図の右側の運動領域となり、T1は長く、T2は短くなります。

【図2】緩和時間と分子運動性(τ c:回転相関時間)
それぞれの緩和時間について、測定法と利用方法を【表1】にまとめました。T1は、定量測定での待ち時間の決定や、分子運動性の解析に利用されます。T2は主にTD-NMR(パルスNMR)において、分子運動性の解析でよく利用されています。
| 緩和時間 | 測定手法 | 利用方法 |
|---|---|---|
| T1緩和時間 | 反転回復法、飽和回復法 | ・定量測定時の待ち時間の決定 ・分子運動性の解析 |
| T2緩和時間 | CPMG法 ハーンエコー法 ソリッドエコー法 |
・分子運動性の解析(TD-NMR) |
【表1】の測定手法のうち、ここでは反転回復法、飽和回復法、CPMG法について紹介します。
2.緩和時間測定手法
① T1緩和時間測定
1) 反転回復法(Inversion Recovery法)
反転回復法は、180°パルスを照射後、τ 秒待ち、その後90°パルスを照射してFIDを取得し、T1を算出する手法です【図3】。

【図3】反転回復法のパルスシークエンス
τ (秒)を少しずつ変化させながら測定すると、信号強度は以下の式に従い【図4】のように変化します(M0 :最大の信号強度)。
Mz (τ)=M0 {1--2exp(-τ ⁄ T1 )}
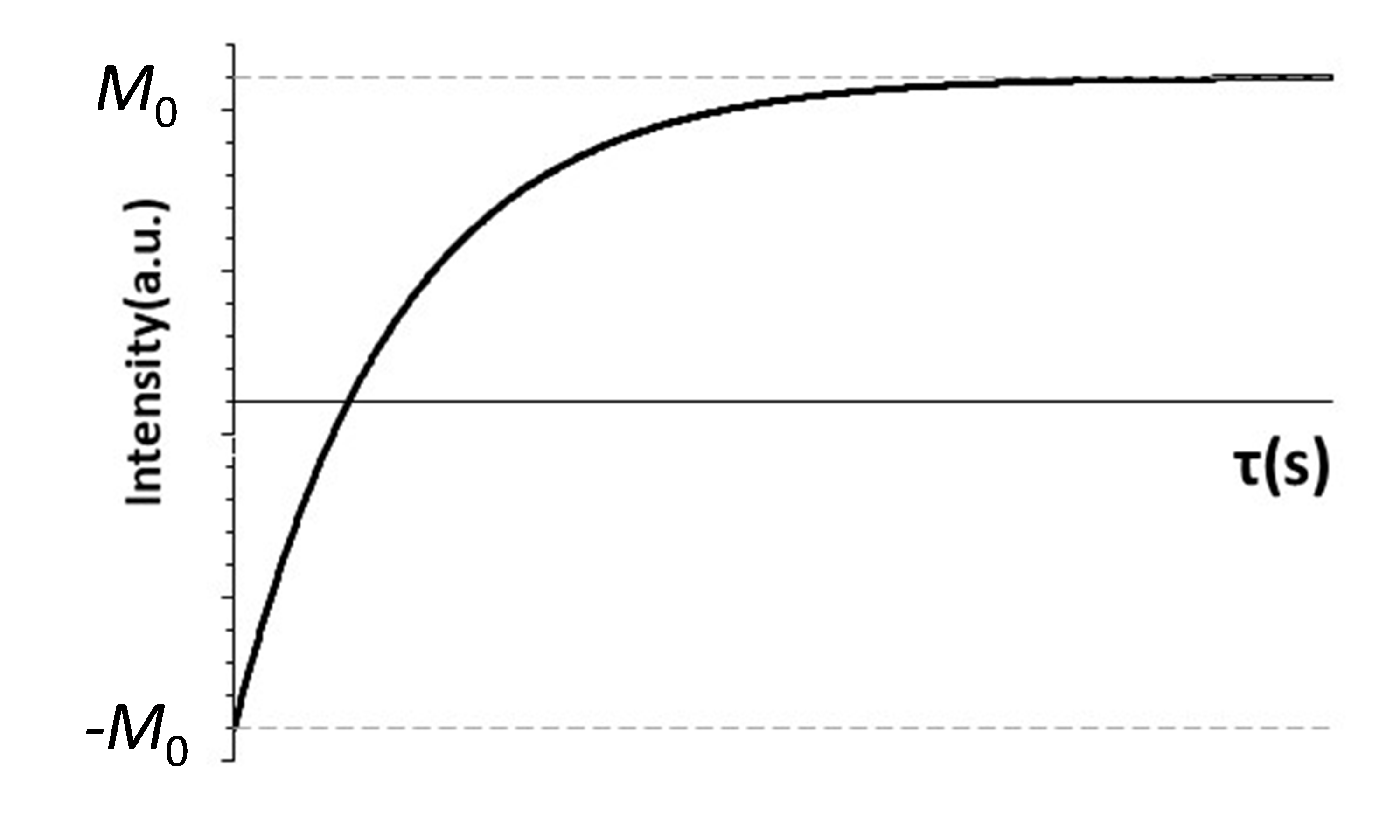
【図4】反転回復法での信号強度変化
各τ における信号強度を上記の式でフィッティングすることでT1を算出します。
反転回復法では信号検出後の待ち時間を長く取り、完全に熱平衡状態まで待つ必要があります。精度の高い測定手法ですが、T1が長い場合、測定に長時間を要することがあります。
例として、N,N-ジメチルアセトアミド(DMA)の1H反転回復法(溶液NMR)の測定結果を【図5】に示します。
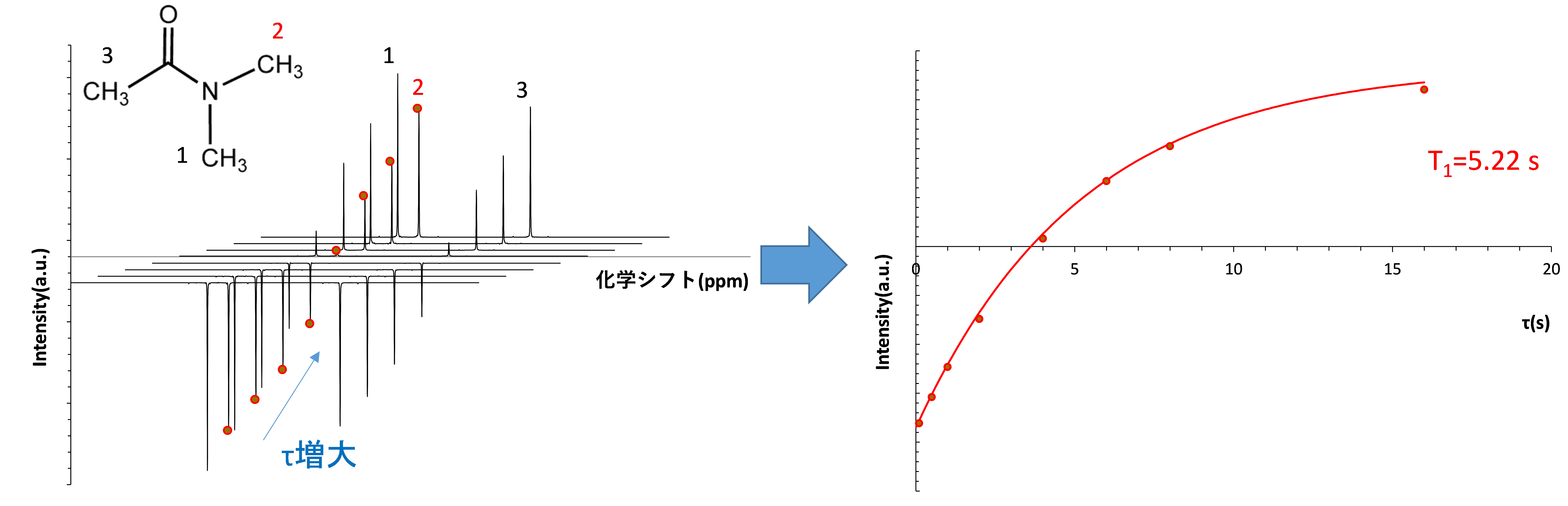
【図5】DMAのCH3基(2)のT1H解析結果(τ =0.1s~16s)
2) 飽和回復法(Inversion Recovery法)
飽和回復法は、始めに飽和パルスを照射、τ 秒待った後に90°パルスを照射してFIDを取得し、T1を算出する手法です【図6】。

【図6】飽和回復法のパルスシークエンス
τ (秒)を少しずつ変化させながら測定すると、信号強度は以下の式に従い【図7】のように変化します。
Mz (τ)=M0 {1-exp(-τ ⁄ T1 )}
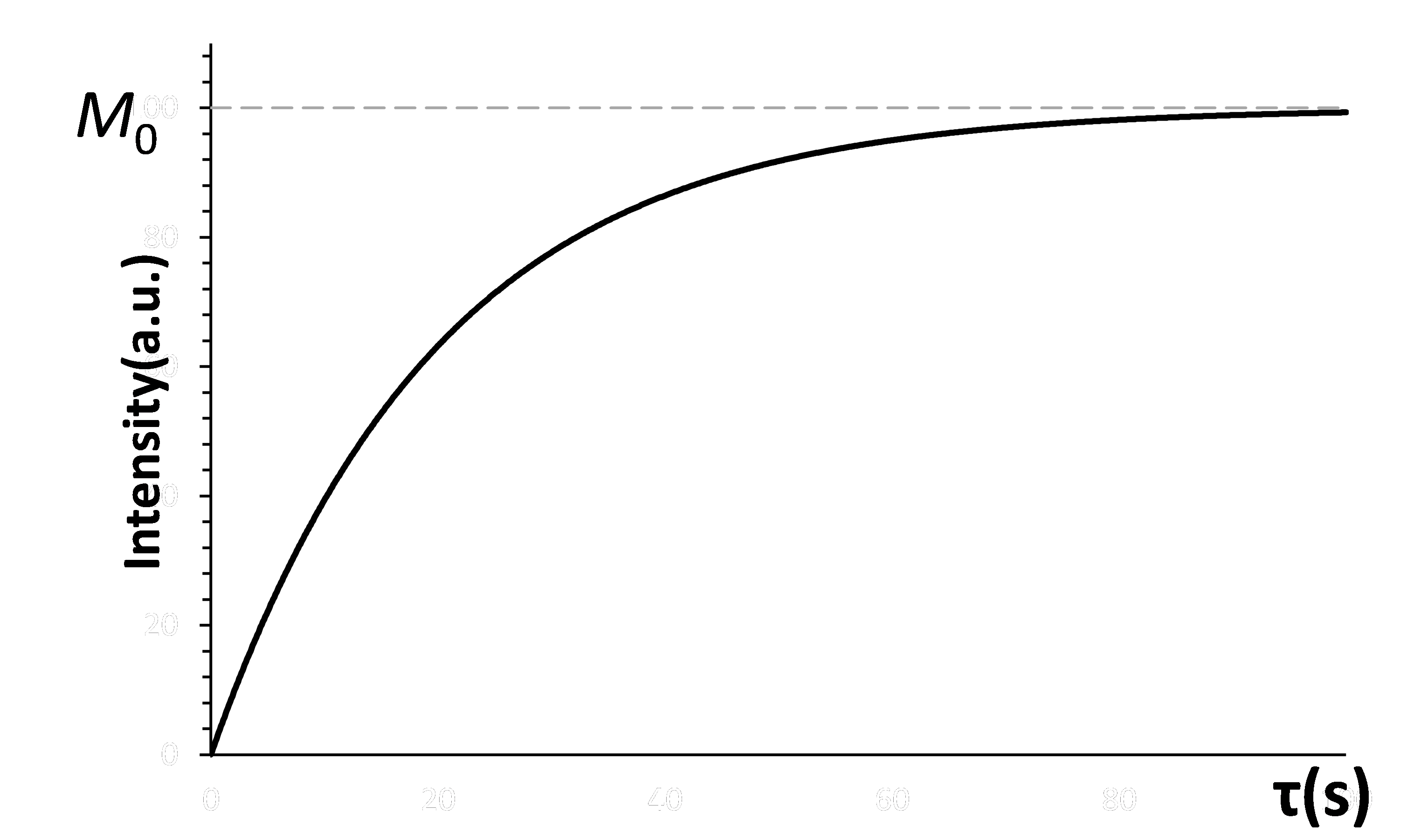
【図7】飽和回復法での信号強度変化
飽和回復法では最初に飽和パルスを照射し磁化を0にするため、待ち時間で熱平衡状態を待つ必要がなく、短い時間に設定できます。しかし、反転回復法に比べT1の測定精度は劣ります。
例として、アダマンタン粉末の1H飽和回復法(固体NMR)の測定結果を【図8】に示します。固体材料ではT1緩和時間が長い場合があり(29Si等)、待ち時間を短く設定できる飽和回復法が有用です。
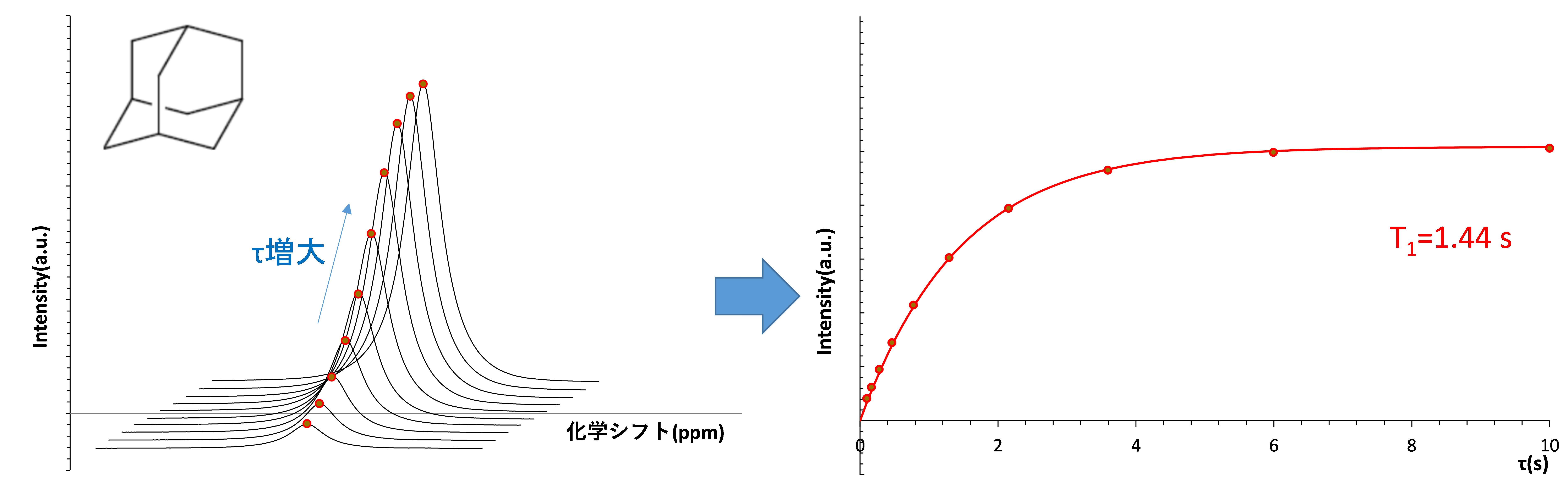
【図8】アダマンタン粉末のT1H測定・解析結果(τ =0.1s~10s、MAS = 7kHz)
② T2緩和時間測定
1) CPMG法(Carr-Purcell-Meiboom-Gill法)
CPMG法は、始めに90°パルスを照射し、その後(τ 秒/180°パルス/τ 秒)のシークエンスをn回繰り返した後FIDを取得し、T2を算出する手法です【図9】。180°パルスの照射を繰り返している間、巨視的磁化はxy平面に固定されます。固定する時間を長くするほどT2緩和が進み、信号強度は小さくなります。
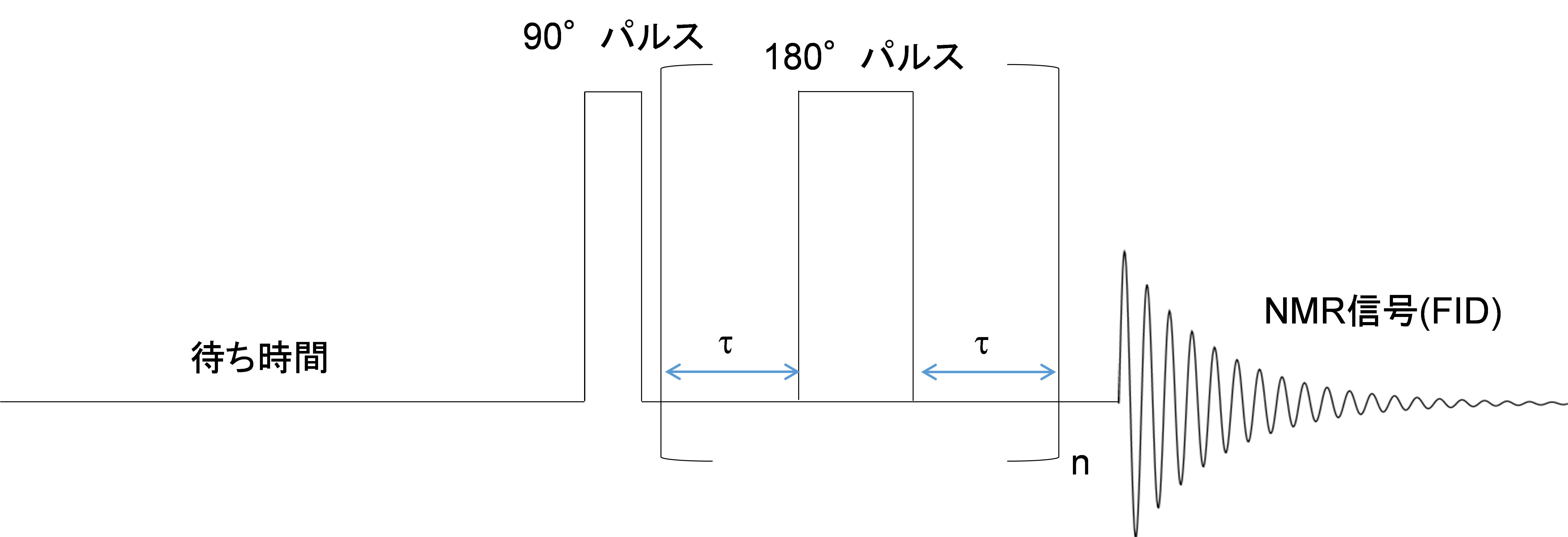
【図9】CPMG法のパルスシークエンス
信号強度の減少は、2nτ (秒)に対して以下の式で表され、【図10】のように変化します。
Mz (2nτ)=M0 {-exp(-2n τ⁄T2 )}
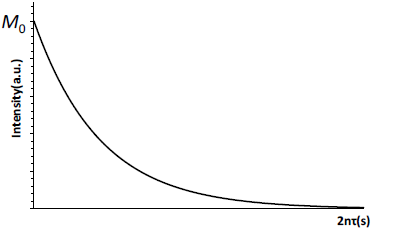
【図10】CPMG法での信号強度変化
例として、DMAの1H CPMG測定結果(溶液NMR)を【図11】に示します。CH3基(2)のT2は4.83sとなり、【図5】で算出したT1(5.22s)に近い値でした。このように、分子運動性の高い試料ではT1とT2が近い値となります。
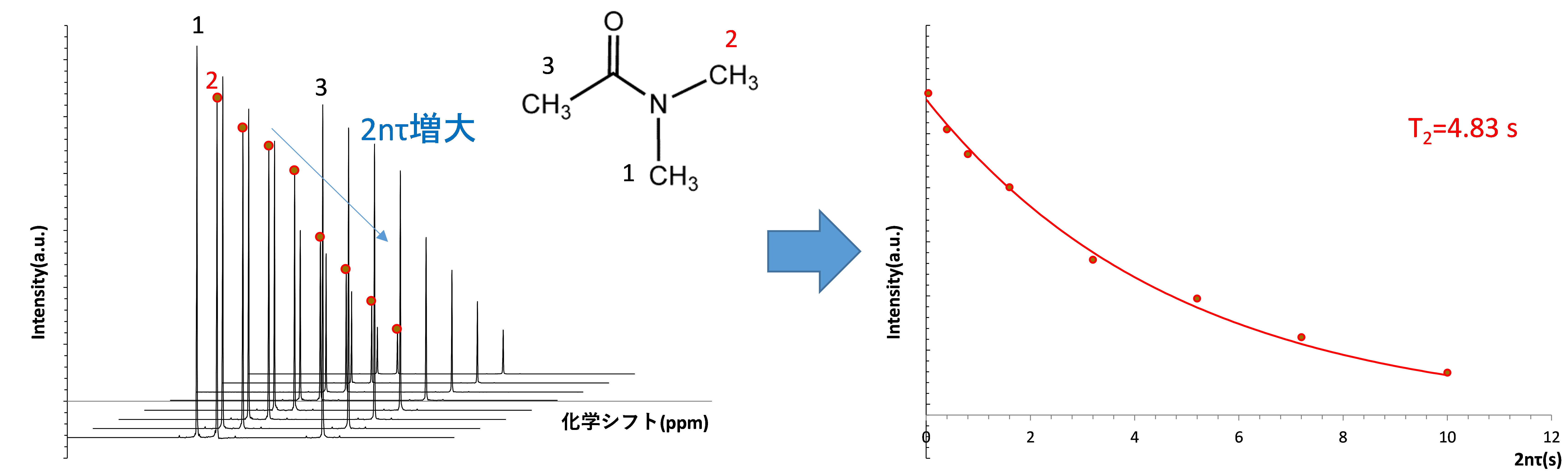
【図11】DMAのCH3基(2)のT2解析結果(2nτ =0.04s~10s)
2) その他のT2測定手法
CPMG法以外のT2測定手法としては、ハーンエコー法やソリッドエコー法が挙げられ、T2の値に応じてこれらの測定手法が使い分けられています【表2】。
分子運動性が低いほどT2は短くなるため、その性質を利用し、材料の分子運動性評価に用いられています。弊社では材料の分子運動性評価に特化したTD-NMR装置(A2203)を導入しています。
|
測定手法 |
T2の領域 |
対象となる材料 |
|
CPMG法 |
数ms~ |
ゲル、溶液等 |
|
ハーンエコー法 |
1~数ms |
ゴム等の柔らかい固体材料 |
| ソリッドエコー法 |
<1ms |
硬い固体材料 |
参考文献
| (1) | T. D. W. Claridge 著、「有機化学のための高分解能NMRテクニック」、竹内敬人、西川実希 訳、講談社サイエンティフィク(2004) |
