概要
本技術資料では、示差走査熱量計(DSC)を用いた小沢法によりエポキシ樹脂の架橋反応における活性化エネルギーを算出した事例を紹介します (1) 。
活性化エネルギー
分解や反応の進みやすさを予め把握しておくことは、目的とする試料を得るためだけでなく、安全確保のためにも重要です。化学反応は出発状態から遷移状態を経て最終状態に到達しますが、一般的に遷移状態は全反応過程の中で最も高いエネルギー準位を有しています。そのため、反応を進行させるためには、遷移状態の高エネルギー状態まで励起させるためのエネルギー(活性化エネルギー)を与える必要があります。この活性化エネルギーの算出方法の1つに、小沢法による速度論的解析があります。
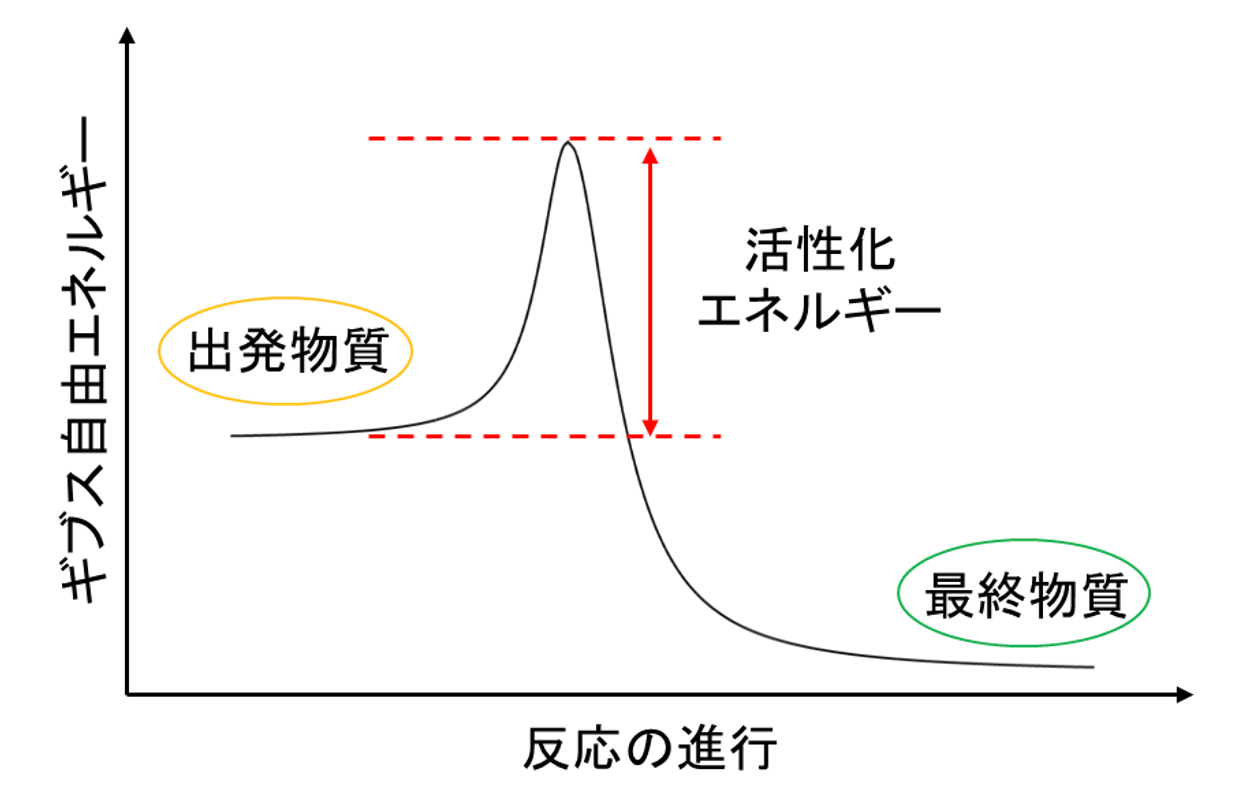
小沢法による解析
小沢法で活性化エネルギーを評価するには昇温速度を変えて複数回DSC測定を行います。その際に得られた吸熱ピークから、各温度における反応率を求め、一定の反応率に到達する温度と、その際の昇温速度を用い、以下の小沢が導いた次の式を用いて活性化エネルギーを算出します(2)。
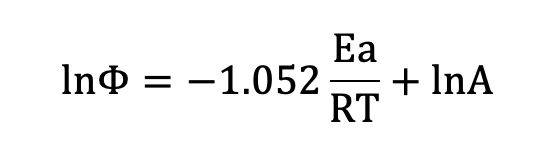
ここで、記号はそれぞれΦ:昇温速度、Ea:活性化エネルギー、R:気体定数、T:絶対温度、A:頻度因子(定数)を表し、Φの自然対数lnΦを1/Tに対してプロットしたグラフの傾きは-1.052Ea/Rとなり、活性化エネルギーEaを算出することができます。
ただし、小沢法では単一の反応にのみ適応可能です。
試料
エポキシ樹脂/硬化剤の混合物
分析方法
装置 : 示差走査熱量計 DSC Q2000 (TA Instruments社製)
条件 : 昇温速度5℃/min、10℃/min、20℃/min、40℃/minの4条件
結果
図2に各昇温速度におけるDSC測定結果を示します。
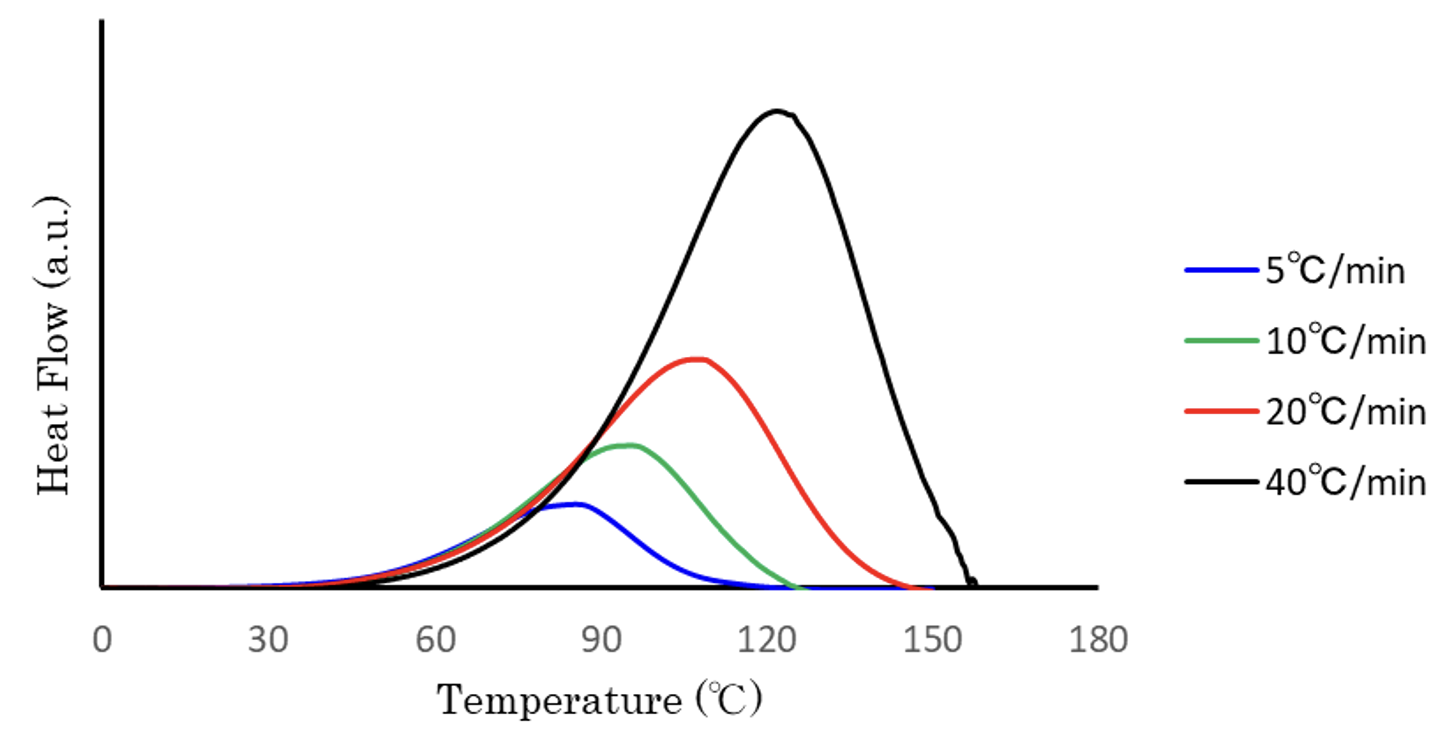
得られたピーク面積から、各反応率に対応する温度を求め、lnΦと絶対温度Tの逆数の関係をプロットしたグラフを図3に示します。
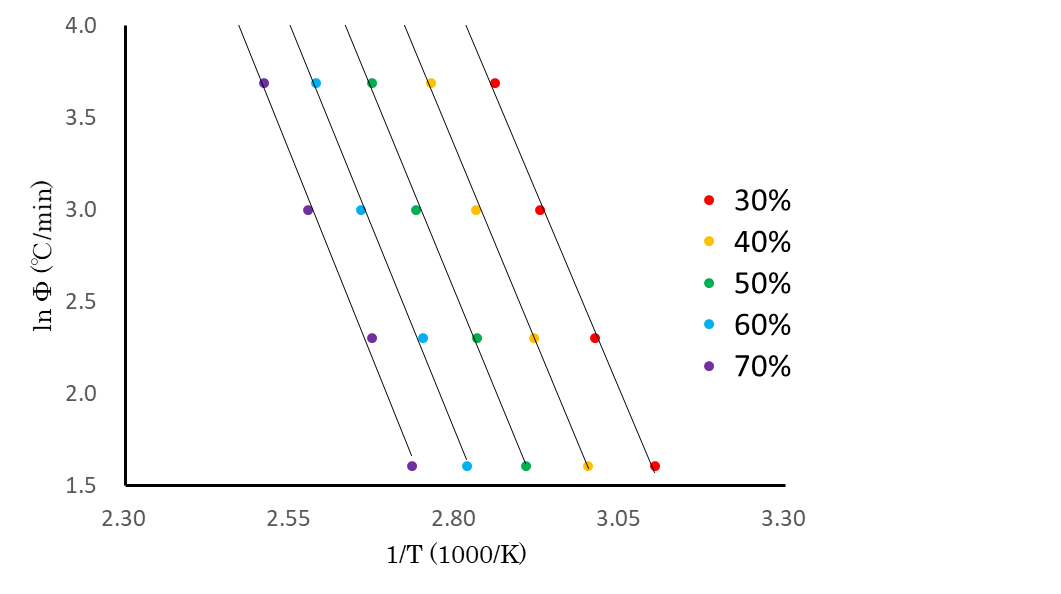
図3から、これらのプロットは直線になっており、かつ各反応率における傾きはほぼ一定となっていることが分かります。これらの傾きから活性化エネルギーを算出すると平均68.9 kJ/molとなりました。
本手法は複数回の試験を行わなければなりませんが、比較的簡便に反応の活性化エネルギーを求める事ができ、エポキシの架橋反応の進み方、安全性に関する知見を得る事が出来ます。
引用文献
- 1) T. Ozawa: Bull. Chem. Soc. Jpn., 38, 1881 (1965)
- 2) 文献(1)の(10)式参照
